Müəllif:
Sara Rhodes
Yaradılış Tarixi:
12 Fevral 2021
YeniləMə Tarixi:
18 Sentyabr 2024

MəZmun
- Addımlar
- Metod 3: pH nədir
- Metod 2 /3: Bilinən Konsentrasiyadan pH hesablayın
- Metod 3 -dən 3: Bilinən pH -dan Konsentrasiyanı Hesablayın
- İpuçları
Gündəlik həyatda pH ümumiyyətlə neytrallığı və ya əksinə bir maddənin neytrallığının olmamasını təsvir etmək üçün istifadə edilən bir miqyas olaraq başa düşülür. Elmi baxımdan, pH dəyəri kimyəvi məhluldakı ionların miqdarına uyğundur. Kimya və ya əlaqəli fənləri öyrənirsinizsə, həll olunan maddələrin konsentrasiyasına əsaslanaraq pH səviyyəsini hesablamalı ola bilərsiniz. PH dəyəri aşağıdakı düsturla tapılır: pH = -lg [H3O].
Addımlar
Metod 3: pH nədir
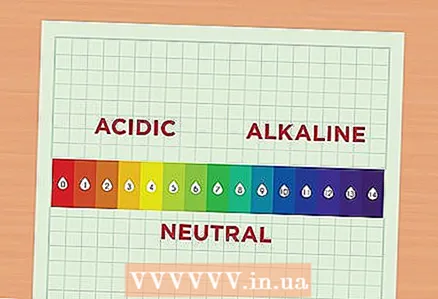 1 PH haqqında məlumat əldə edin. PH dəyəri məhlulda hidrogen ionlarının konsentrasiyasına uyğundur. Hidrogen ionlarının konsentrasiyası artan bir həll turş, bu ionların konsentrasiyası aşağı olan məhlulu isə qələvi adlanır. Hidrogen ionları qısaca olaraq H olaraq təyin olunur. Bir birləşmənin bir hissəsi olaraq da təqdim edilə bilər, sonra hidronium adlanır və H olaraq yazılır.30.
1 PH haqqında məlumat əldə edin. PH dəyəri məhlulda hidrogen ionlarının konsentrasiyasına uyğundur. Hidrogen ionlarının konsentrasiyası artan bir həll turş, bu ionların konsentrasiyası aşağı olan məhlulu isə qələvi adlanır. Hidrogen ionları qısaca olaraq H olaraq təyin olunur. Bir birləşmənin bir hissəsi olaraq da təqdim edilə bilər, sonra hidronium adlanır və H olaraq yazılır.30. - PH şkalasını oxuyun. PH şkalası 1 ilə 14 arasında dəyişir. Sayı nə qədər aşağı olarsa, həll daha asidik olar. Əksinə, dəyər nə qədər yüksəkdirsə, həll bir o qədər qələvidir. Məsələn, portağal suyunun pH -ı 2 -dir, çünki bu meyvə kifayət qədər asidik bir mayedir. Xlorlu ağartıcının tərkibində çoxlu qələvi olduğu üçün pH 12 -dir. Ölçünün ortasında pH 7 olan su kimi nisbətən neytral həllər var.
- PH ölçüsündə iki həll arasındakı 1 ballıq fərq, turşuluq baxımından 10 qat fərqləndikləri mənasına gəlir. Məsələn, pH 6 və 7 olan iki həll alsanız, pH 6 olan birinci məhlulun turşuluğu, pH 7 olan ikinci məhlulun turşuluğundan 10 qat yüksək olacaq. Və məsələn, pH 6 olan bir məhlulun turşuluğu, pH 8 olan məhlulun turşuluğundan 100 dəfə çoxdur.
 2 PH təyin etmək üçün tənliyi əzbərləyin. PH miqyası mənfi ondalık logarifması ilə hesablanır. Mənfi ondalık logarifması sıfır tam ədədlər daxil olmaqla birindən əvvəlki sıfır sayına uyğundur: məsələn, 0.1 -in mənfi onluq loqarifması 1 -dir, 0.01 -i 2 -dir və s. PH tapmaq üçün düstur belədir: pH = -lg [H3O].
2 PH təyin etmək üçün tənliyi əzbərləyin. PH miqyası mənfi ondalık logarifması ilə hesablanır. Mənfi ondalık logarifması sıfır tam ədədlər daxil olmaqla birindən əvvəlki sıfır sayına uyğundur: məsələn, 0.1 -in mənfi onluq loqarifması 1 -dir, 0.01 -i 2 -dir və s. PH tapmaq üçün düstur belədir: pH = -lg [H3O]. - Bəzən düstur pH = -lg [H] olaraq yazılır. H tənliyinin olub -olmamasının əhəmiyyəti yoxdur3O və ya H, hər ikisi ekvivalentdir.
- PH tapmaq üçün ondalık logarifmini hesablaya bilmək lazım deyil, çünki demək olar ki, hər bir elmi və ya mühəndislik kalkulyatorunda hesablamaq imkanı var.
 3 Konsentrasiya haqqında məlumat əldə edin. Bir maddənin konsentrasiyası, bu maddənin həllində olan hissəciklərin sayına uyğun gəlir. Bir qayda olaraq, konsentrasiya vahid həcmdə mol sayında ifadə olunur və m / V və ya M. olaraq ifadə edilir. Kimya laboratoriyalarında məhlulların konsentrasiyası onlarla şüşələrdə yazılır. Kimyəvi bir problemi həll edirsinizsə, konsentrasiya bu vəziyyətdə verilə bilər və ya tapılmalıdır.
3 Konsentrasiya haqqında məlumat əldə edin. Bir maddənin konsentrasiyası, bu maddənin həllində olan hissəciklərin sayına uyğun gəlir. Bir qayda olaraq, konsentrasiya vahid həcmdə mol sayında ifadə olunur və m / V və ya M. olaraq ifadə edilir. Kimya laboratoriyalarında məhlulların konsentrasiyası onlarla şüşələrdə yazılır. Kimyəvi bir problemi həll edirsinizsə, konsentrasiya bu vəziyyətdə verilə bilər və ya tapılmalıdır.
Metod 2 /3: Bilinən Konsentrasiyadan pH hesablayın
 1 PH tapma formulunu xatırlayın. Budur düstur: pH = -lg [H3O]. Bu formulu təşkil edən bütün elementlərlə tanış olduğunuzdan əmin olun. Hansı dəyərin konsentrasiyaya uyğun olduğunu görün.
1 PH tapma formulunu xatırlayın. Budur düstur: pH = -lg [H3O]. Bu formulu təşkil edən bütün elementlərlə tanış olduğunuzdan əmin olun. Hansı dəyərin konsentrasiyaya uyğun olduğunu görün. - Kimyada kvadrat mötərizələr bir şeyin konsentrasiyası deməkdir.Beləliklə, pH hesablama formulu "pH hidronium ion konsentrasiyasının mənfi logarifmasına bərabərdir" yazır.
 2 Həqiqi konsentrasiyanı təyin edin. Problem ifadəsini diqqətlə oxuyun. Mənbə məlumatlarında turşu və ya qələvi konsentrasiyasını tapın. Bilinən dəyərləri əvəz edərək tam bir düsturu bir kağıza yazın. Qarışıqlığın qarşısını almaq üçün həmişə ədədlərin yanında ölçü vahidlərini göstərin.
2 Həqiqi konsentrasiyanı təyin edin. Problem ifadəsini diqqətlə oxuyun. Mənbə məlumatlarında turşu və ya qələvi konsentrasiyasını tapın. Bilinən dəyərləri əvəz edərək tam bir düsturu bir kağıza yazın. Qarışıqlığın qarşısını almaq üçün həmişə ədədlərin yanında ölçü vahidlərini göstərin. - Məsələn, konsentrasiyası 1.05 x 10 M olarsa, pH hesablama formulunu belə yazın: pH = -lg [1.05 x 10 M]
 3 PH hesablayın. Bunun üçün elmi bir kalkulyatordan istifadə etmək rahatdır. Əvvəlcə "+/-" düyməsini basaraq eksi işarəsini daxil edin. Sonra ondalık logarifmaya uyğun olan "log" düyməsini basın (İngilis dilində ondalık logarifma log adlanır). Ekranda "-log" göstərilir. Sonra sol mötərizəni basın və konsentrasiyanı daxil edin. Gerekirse dərəcənin dəyərini göstərməyi unutmayın. Sonra mötərizələri bağlayın. Nəticədə, kalkulyator ekranında “-log (1.05x10) görürsünüz. "=" Düyməsini basın. PH dəyəriniz təxminən 4.98 olmalıdır.
3 PH hesablayın. Bunun üçün elmi bir kalkulyatordan istifadə etmək rahatdır. Əvvəlcə "+/-" düyməsini basaraq eksi işarəsini daxil edin. Sonra ondalık logarifmaya uyğun olan "log" düyməsini basın (İngilis dilində ondalık logarifma log adlanır). Ekranda "-log" göstərilir. Sonra sol mötərizəni basın və konsentrasiyanı daxil edin. Gerekirse dərəcənin dəyərini göstərməyi unutmayın. Sonra mötərizələri bağlayın. Nəticədə, kalkulyator ekranında “-log (1.05x10) görürsünüz. "=" Düyməsini basın. PH dəyəriniz təxminən 4.98 olmalıdır.
Metod 3 -dən 3: Bilinən pH -dan Konsentrasiyanı Hesablayın
 1 Nə verildiyini və nə tapmaq istədiyinizi müəyyənləşdirin. PH hesablamaq üçün düsturu yazın. Sonra düsturun altına dəyərlərini yazaraq bilinən dəyərləri anlayın. Məsələn, pH'ınızın 10.1 olduğunu bilirsinizsə, bu rəqəmi düsturunuzdakı pH altında yazın.
1 Nə verildiyini və nə tapmaq istədiyinizi müəyyənləşdirin. PH hesablamaq üçün düsturu yazın. Sonra düsturun altına dəyərlərini yazaraq bilinən dəyərləri anlayın. Məsələn, pH'ınızın 10.1 olduğunu bilirsinizsə, bu rəqəmi düsturunuzdakı pH altında yazın.  2 Formulu çevirin. Bu vəziyyətdə, məktəb cəbr kursundan biliklərə ehtiyacınız olacaq. Bilinən pH dəyərindən konsentrasiyanı hesablamaq üçün düsturu, konsentrasiyanın tənliyin hər iki tərəfindən ayrı durması üçün çevirmək lazımdır. Yəni bərabər işarənin bir tərəfində pH dəyərini, digər tərəfində isə hidronium konsentrasiyasını ehtiva edən bir ifadə olması lazımdır. Əvvəlcə tənliyin hər iki tərəfini -1 ilə vurun. Sonra ortaya çıxan bərabərliyin hər iki tərəfindəki güclərə 10 yüksəldin.
2 Formulu çevirin. Bu vəziyyətdə, məktəb cəbr kursundan biliklərə ehtiyacınız olacaq. Bilinən pH dəyərindən konsentrasiyanı hesablamaq üçün düsturu, konsentrasiyanın tənliyin hər iki tərəfindən ayrı durması üçün çevirmək lazımdır. Yəni bərabər işarənin bir tərəfində pH dəyərini, digər tərəfində isə hidronium konsentrasiyasını ehtiva edən bir ifadə olması lazımdır. Əvvəlcə tənliyin hər iki tərəfini -1 ilə vurun. Sonra ortaya çıxan bərabərliyin hər iki tərəfindəki güclərə 10 yüksəldin. - PH = -log bərabərliyini çevirmək [H3O], + [H formulunu əldə edirik3O] = 10, yəni ion konsentrasiyası -pH gücünə ondur. İndi pH əvəzinə, bizim vəziyyətimizdə 10.1 olan bilinən bir dəyəri əvəz edirik.
 3 Tənliyi həll edin. Kalkulyatorda onu bir gücə qaldırmaq üçün xüsusi bir prosedur var. Əvvəlcə 10 yazın. Sonra eksponentasiya düyməsini basın. Eksi işarəsi və dərəcə dəyəri daxil edin. "=" Düyməsini basın.
3 Tənliyi həll edin. Kalkulyatorda onu bir gücə qaldırmaq üçün xüsusi bir prosedur var. Əvvəlcə 10 yazın. Sonra eksponentasiya düyməsini basın. Eksi işarəsi və dərəcə dəyəri daxil edin. "=" Düyməsini basın. - Bizim nümunəmizdə pH 10.1 -dir. "10" yığın və "EXP" düyməsini basın. Sonra işarəni dəyişdirərək "- / +" düyməsini basın. Nəhayət, pH dəyərini "10.1" daxil edin və "=" düyməsini basın. Nəticədə 1e-100 ilə sona çatmalısınız. Bu, konsentrasiyanın 1.00 x 10 M olması deməkdir.
 4 Aldığınız cavabı düşünün. Fiziki mənası varmı? Əgər pH 10.1 olarsa, bu, hidroniumun konsentrasiyasının son dərəcə aşağı olması və qələvi məhlulunuz olması deməkdir. Beləliklə, tapılan çox aşağı konsentrasiyaya uyğundur
4 Aldığınız cavabı düşünün. Fiziki mənası varmı? Əgər pH 10.1 olarsa, bu, hidroniumun konsentrasiyasının son dərəcə aşağı olması və qələvi məhlulunuz olması deməkdir. Beləliklə, tapılan çox aşağı konsentrasiyaya uyğundur
İpuçları
- PH səviyyənizi hesablamaq əvvəlcə çətindirsə, mövzu haqqında daha çox məlumat əldə etmək üçün bir çox mənbənin olduğunu unutmayın. Kimya dərsliyindən istifadə edin və ya müəllimdən kömək istəyin.