Müəllif:
Judy Howell
Yaradılış Tarixi:
27 İyul 2021
YeniləMə Tarixi:
23 İyun 2024

MəZmun
- Addımlamaq
- 4-dən 1-ci hissə: Quruluşu anlamaq
- 4-dən 2-ci hissə: simvolu anlamaq və adlandırma
- 4-ün 3-cü hissəsi: Atom nömrəsini oxumaq
- 4-dən 4-cü hissə: Atom kütləsinin oxunması
Elementlərin dövri cədvəli bu günə qədər aşkar edilmiş 118 elementin siyahısıdır. Elementlərdəki fərqləri göstərən bir neçə simvol və rəqəm var, cədvəlin quruluşu elementləri oxşarlıqlarına görə təşkil edir. Aşağıdakı təlimatlardan istifadə edərək dövri cədvəli oxuya bilərsiniz.
Addımlamaq
4-dən 1-ci hissə: Quruluşu anlamaq
 Dövri cədvəli sanki sol üstdən başlayır və sonuncu sətrin sonunda, altda və sağda bitir. Cədvəl artan atom sayına görə soldan sağa qurulmuşdur. Atom nömrəsi tək bir atomun içindəki proton sayıdır.
Dövri cədvəli sanki sol üstdən başlayır və sonuncu sətrin sonunda, altda və sağda bitir. Cədvəl artan atom sayına görə soldan sağa qurulmuşdur. Atom nömrəsi tək bir atomun içindəki proton sayıdır. - Hər sətir və ya sütun tam deyil. Mərkəzdə boşluqlar ola bilsə də, cədvəli soldan sağa oxumağa davam edin. Məsələn, hidrogen atom nömrəsinə 1 sahibdir və yuxarı sol küncdə yerləşir. Heliumun atom nömrəsi 2 var və yuxarı sağ küncdədir.
- 57 ilə 71 arasındakı elementlər ümumiyyətlə cədvəlin sağ alt küncündə bir alt kimi təsvir olunur. Bunlar "nadir torpaq elementləri" dir.
 Cədvəlin hər sütununda bir element qrupu tapacaqsınız. 18 sütun var.
Cədvəlin hər sütununda bir element qrupu tapacaqsınız. 18 sütun var. - Yuxarıdan aşağıya oxumaq üçün "bir qrupu oxumaq" ifadəsini istifadə edin.
- Nömrələmə ümumiyyətlə sütunların üstündə göstərilir; bununla yanaşı metal kimi digər qruplar altında da ola bilər.
- Dövri cədvəldə istifadə olunan nömrələmə çox fərqlənir. Roman (IA), ərəb (1A) və ya 1 ilə 18 arasında rəqəmlər ola bilər.
- Hidrogen, halogen ailəsində və Qələvi metallarda və ya hər ikisində ola bilər.
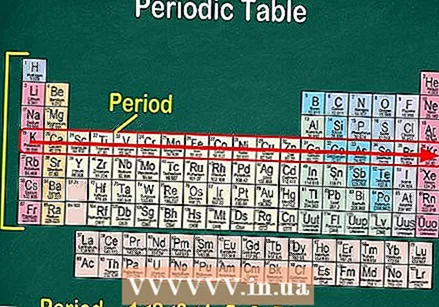 Cədvəlin hər sətrində elementlərin "dövrlərini" tapacaqsınız. 7 dövr var. Soldan sağa oxumaq üçün "bir müddət boyunca oxuyun" ifadəsini istifadə edin.
Cədvəlin hər sətrində elementlərin "dövrlərini" tapacaqsınız. 7 dövr var. Soldan sağa oxumaq üçün "bir müddət boyunca oxuyun" ifadəsini istifadə edin. - Dövrlər ümumiyyətlə masanın sol tərəfində 1 ilə 7 arasında nömrələnir.
- Hər dövr sonuncudan daha böyükdür. Bu, dövri sistemdəki atomların enerji səviyyələrinin artırılması ilə əlaqədardır.
 Metal, yarı metal və metal olmayan əlavə qrupları anlayın. Rənglər çox fərqlidir.
Metal, yarı metal və metal olmayan əlavə qrupları anlayın. Rənglər çox fərqlidir. - Metallar qrupu bir rəngə malikdir. Bununla birlikdə, hidrogen çox vaxt qeyri-metallarla eyni rəngə və qrupa sahibdir. Metallar parıldayır, ümumiyyətlə otaq temperaturunda qatıdır, istilik və elektrik enerjisi keçirir, mülayim və yumşaqdır.
- Qeyri-metal eyni rəngə sahibdir. Bunlar H-1 (hidrogen) daxil olmaqla C-6-dan Rn-86-dək elementlərdir. Parıltıları yoxdur, istilik və elektrik keçirir və dözümlü deyillər. Ümumiyyətlə otaq temperaturunda bir qaz meydana gətirirlər və qatı, qaz və ya maye ola bilərlər.
- Yarı metal / metalloidlər, adətən, digər iki rəngin birləşməsi kimi bənövşəyi və ya yaşıl rəngə malikdirlər. Xətt B-5 elementlərindən At-85-ə qədər uzanan diaqonaldır. Metalların bəzi və qeyri-metalların bəzi xüsusiyyətləri var.
 Qeyd edək ki, elementlər bəzən ailələrdə də sadalanır. Bunlar qələvi metallar (1A), qələvi torpaq metalları (2A), halogenlər (7A), nəcib qazlar (8A) və karbon atomlarıdır (4A).
Qeyd edək ki, elementlər bəzən ailələrdə də sadalanır. Bunlar qələvi metallar (1A), qələvi torpaq metalları (2A), halogenlər (7A), nəcib qazlar (8A) və karbon atomlarıdır (4A). - Nömrələmə Roman, Ərəb və ya standart nömrələr ola bilər.
4-dən 2-ci hissə: simvolu anlamaq və adlandırma
 Əvvəlcə simvolu oxuyun. Bir və ya iki hərfdən ibarətdir və bir neçə dildə standartdır.
Əvvəlcə simvolu oxuyun. Bir və ya iki hərfdən ibarətdir və bir neçə dildə standartdır. - Rəmz elementin Latın adından və ya ümumi ortaq məxrəcdən əldə edilə bilər.
- Bir çox halda, simvol Helium və ya "He" kimi ingilis adlandırma konvensiyasını izləyir. Bununla birlikdə, fərz edə biləcəyiniz bir qayda deyil. Məsələn, dəmir "Fe" dir. Bu səbəbdən simvol / ad birləşməsi ümumiyyətlə sürətli müraciət üçün xatırlanır.
 Ümumi ada baxın. Bu birbaşa simvolun altındadır. Bu, dövri cədvəlin yazıldığı dildən asılı olaraq fərqlənir.
Ümumi ada baxın. Bu birbaşa simvolun altındadır. Bu, dövri cədvəlin yazıldığı dildən asılı olaraq fərqlənir.
4-ün 3-cü hissəsi: Atom nömrəsini oxumaq
 Hər elementin qutusunun yuxarı mərkəzindəki atom nömrəsinə görə dövri cədvəli oxuyun. Daha əvvəl də qeyd edildiyi kimi, sistem yuxarıdan soldan sağa sifariş edilir. Atom nömrəsini bilmək, element haqqında daha çox məlumat axtarmaq üçün ən sürətli yoldur.
Hər elementin qutusunun yuxarı mərkəzindəki atom nömrəsinə görə dövri cədvəli oxuyun. Daha əvvəl də qeyd edildiyi kimi, sistem yuxarıdan soldan sağa sifariş edilir. Atom nömrəsini bilmək, element haqqında daha çox məlumat axtarmaq üçün ən sürətli yoldur. 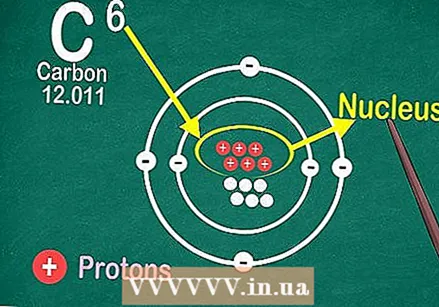 Atom nömrəsi, elementin tək bir atomunun nüvəsindəki proton sayıdır.
Atom nömrəsi, elementin tək bir atomunun nüvəsindəki proton sayıdır. Protonların əlavə edilməsi və ya çıxarılması fərqli bir element yaradır.
Protonların əlavə edilməsi və ya çıxarılması fərqli bir element yaradır. Bir atomdakı proton sayını tapmaq elektron sayını da müəyyənləşdirir. Atomlarda proton qədər elektron var.
Bir atomdakı proton sayını tapmaq elektron sayını da müəyyənləşdirir. Atomlarda proton qədər elektron var. - Bu qaydanın bir istisnasının olduğunu unutmayın. Atom elektron itirəndə və ya qazandıqda, elektrik yüklü bir ion olur.
- Elementin simvolunun yanında bir artı işarəsi varsa, bunun müsbət yükləndiyini göstərir. Eksi işarəsi ilə mənfi yüklənir.
- Artıq və ya mənfi bir simvol yoxdursa və kimya probleminiz ionlarla əlaqəli deyilsə, proton və elektronların sayı yəqin ki bərabərdir.
4-dən 4-cü hissə: Atom kütləsinin oxunması
 Atom kütləsini təyin edin. Bu elementin ümumi adının altındakı rəqəmdir.
Atom kütləsini təyin edin. Bu elementin ümumi adının altındakı rəqəmdir. - Atom kütləsi sistemin yuxarı solundan sağ altına doğru artarkən görünsə də, bu, bütün hallarda doğru deyil.
 Əksər elementlərin ondalık rəqəmlərlə təmsil olunduğunu anlayın. Atom kütləsi nüvədəki hissəciklərin cəmidir; Bununla birlikdə, fərqli izotopların ağırlıqlı ortalamasıdır.
Əksər elementlərin ondalık rəqəmlərlə təmsil olunduğunu anlayın. Atom kütləsi nüvədəki hissəciklərin cəmidir; Bununla birlikdə, fərqli izotopların ağırlıqlı ortalamasıdır.  Tək bir atomdakı neytronların sayını tapmaq üçün atom kütləsindən istifadə edin. Atom kütləsini ən yaxın tam ədədə, kütlə sayına qədər yuvarlaqlaşdırın. Daha sonra neytronların sayını təyin etmək üçün kütlə sayından proton sayını çıxardırsınız.
Tək bir atomdakı neytronların sayını tapmaq üçün atom kütləsindən istifadə edin. Atom kütləsini ən yaxın tam ədədə, kütlə sayına qədər yuvarlaqlaşdırın. Daha sonra neytronların sayını təyin etmək üçün kütlə sayından proton sayını çıxardırsınız. - Məsələn: Dəmirin atom kütləsi 55.847, kütlə sayı 56. Elementin 26 protonu var. 56 (kütlə sayı) mənfi 26 (protonlar) 30-dur. Tək bir dəmir atomunda ümumiyyətlə 30 neytron olur.
- Atomdakı neytronların sayının dəyişdirilməsi, atomun daha ağır və ya daha yüngül versiyaları olan izotoplar meydana gətirir.



