Müəllif:
Monica Porter
Yaradılış Tarixi:
17 Mart 2021
YeniləMə Tarixi:
1 İyul 2024

MəZmun
Molyar konsentrasiya bir həll olunan maddənin mol sayı ilə məhlulun həcmi arasındakı əlaqəni göstərir. Molyarlığı hesablamaq üçün mol və həcm, kütlə və həcm və ya mol və mililitr (ml) ilə başlaya bilərsiniz. Sonra yuxarıdakı dəyişənlərlə birlikdə düzgün nəticə əldə etmək üçün əsas molar konsentrasiyası formulunu tətbiq edin.
Addımlar
Metod 4-dən 1: Molar Sayı və Həcmdən Mol Konsentrasiyasını hesablayın
Molyar konsentrasiyanı hesablamaq üçün əsas düsturu bilmək vacibdir. Bir həll olunan maddənin mol sayına, məhlul həcminin litrə bölünməsinə bərabər olan molar konsentrasiya. Oradan aşağıdakı düsturumuz var: Molyar konsentrasiyası = həll olunan molların sayı / litr həll miqdarı
- Misal: 4.2 litr məhlulda 0.75 mol NaCl olan məhlulun molyar konsentrasiyası nə qədərdir?

Mövzunu təhlil edin. Molyar konsentrasiyanı hesablamaq üçün mol sayına və litr həcmindəki həll həcminə ehtiyacınız var. Verilən mövzuya görə bu iki dəyəri hesablamağa ehtiyac yoxdur.- Misal üçün:
- Molların sayı = 0.75 mol NaCl
- Həcm = 4.2 L
- Misal üçün:
Mol sayını həcminə bölün. Mol həcminə görə bölünməsinin nəticəsi, bir litr məhlula düşən mol sayı və ya bu məhlulun molar konsentrasiyasıdır.
- Nümunə: molyar konsentrasiyası = həll olunan molun sayı / litr həll miqdarı = 0.75 mol / 4.2 L = 0.17857142

Nəticələrinizi qeyd edin. Müəllimin istəyi və ya tapşırıqdan asılı olaraq, vergüldən sonra iki və ya üç ədədi yuvarlaqlaşdırın. Nəticələrinizi qeyd edərkən "molar konsentrasiyanı" "M" ilə qısaldın və həll olunan maddənin kimyəvi simvolunu daxil edin.- Misal üçün: 0.179 M NaCl
Metod 4-dən 2: Kütlədən və Həcmdən Mol Konsentrasiyasını hesablayın
Molyar konsentrasiyanı hesablamaq üçün əsas düsturu bilmək lazımdır. Molyar konsentrasiya bir həll olunan maddənin mol sayı ilə məhlulun həcmi arasındakı əlaqəni göstərir. Molyar konsentrasiyanın formulu aşağıdakı kimidir: mol konsentrasiyası = həll olunan maddə konsentrasiyası / litr həll sayı
- Problem nümunəsi: 3.4 q KMnO həll edildikdə məhlulun mol sayını hesablayın4 5.2 litr suda.

Mövzunu təhlil edin: Molyar konsentrasiyanı tapmaq üçün mol sayına və litrin həll həcminə ehtiyacınız var. Bu dəyərlər verilmirsə, ancaq məhlulun həcmini və kütləsini bilirsinizsə, molyar konsentrasiyasını hesablamadan əvvəl həll olunan maddənin mol sayını təyin edə bilərsiniz.- Misal üçün:
- Çəki = 3,4 q KMnO4
- Həcmi = 5.2 L
- Misal üçün:
Həll olunan maddənin kütlə molekulunu hesablayın. Bu kütlənin və ya qram həll olunan maddənin mol sayını hesablamaq üçün əvvəlcə maddənin kütlə molekulunu təyin etməlisiniz. Bir həll olunan maddənin kütlə molekulunu məhluldakı hər elementin kütlə atomunu əlavə etməklə təyin etmək olar. Hər bir elementin kub atomunu tapmaq üçün elementlərin dövri cədvəlindən istifadə edin.
- Misal üçün:
- K = 39.1 q kütlə atomu
- Kütlə atomu Mn = 54,9 q
- Kütlə atomu O = 16,0 q
- Kütlənin ümumi atomları = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158,0 q
- Misal üçün:
Qramları mollara çevirin. Bir kub molekuluna sahib olduqdan sonra, məhluldakı həll olunan maddənin qram sayını, həll olunan maddənin molar kütləsi başına 1 mol ekvivalent konversiya əmsalı ilə vurmaq lazımdır. Bu vurmanın nəticəsi həll olunan maddənin mol sayıdır.
- Misal: qram həll olunan maddə * (1 / həll olunan molyar kütlə) = 3.4 g * (1 mol / 158 g) = 0.0215 mol
Mol sayını litr sayına bölün. Artıq mol sayını hesabladığınız üçün bu sayını məhlulun həcminə görə litrə bölün, bu məhlulun molar konsentrasiyasına sahib olacaqsınız.
- Nümunə: molyar konsentrasiya = həll olunan molun miqdarı / məhlul litri sayı = 0.0215 mol / 5.2 L = 0.004134615
Nəticələrinizi qeyd edin. Nəticələri müəllimin tələb etdiyi kimi, ümumiyyətlə vergüldən sonra iki-üç rəqəm yığmalısınız. Bundan əlavə, nəticəni yazarkən "molar konsentrasiyanı" "M" kimi qısaltın və həll olunan maddənin kimyəvi simvolunu müşayiət edin.
- Misal üçün: 0,004 M KMnO4
Metod 4-dən 3: Mol və Mililitr məhlul sayından Molar konsentrasiyasını hesablayın
Molyar konsentrasiyanın formulunu bilmək lazımdır. Molyar konsentrasiyanı hesablamaq üçün. Solüsyonun mililitrini deyil, bir litrə görə həll olunan maddənin mol sayını hesablamalısınız. Molyar konsentrasiyanı hesablamaq üçün ümumi düstur: molyar konsentrasiyası = həll olunan molların sayı / litr həll sayı
- Nümunə: 1.2 mol CaCl olan bir məhlulun molar konsentrasiyasını hesablayın2 2905 mililitr suda.
Mövzunu təhlil edin. Molyar konsentrasiyanı hesablamaq üçün həll olunan molların sayına və litr həcmindəki həll həcminə ehtiyacınız var. Problemdə həll həcmi mililitrlə verilmişdirsə, hesablamadan əvvəl litrlə ekvivalent həcmə çevirin.
- Misal üçün:
- Molların sayı = 1,2 mol CaCl2
- Həcmi = 2905 ml
- Misal üçün:
Mililitrləri litrə çevirin. Solüsyonu mililitrdən litrə çevirmək üçün mililitr sayını 1000-ə bölün, çünki hər litr 1000 mililitrə bərabərdir. Onluq nöqtəni 3 rəqəmi sola dəyişdirərək mililitrləri litrə çevirə bilərsiniz.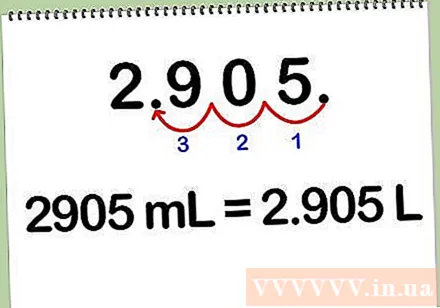
- Məsələn: 2905 ml * (1 L / 1000 ml) = 2,905 L
Mol sayını litr sayına bölün. Litr sayına sahib olduqdan sonra, mol sayını həll litrinin sayına bölərək molar konsentrasiyanı hesablaya bilərsiniz.
- Nümunə: molyar konsentrasiyası = həll olunan molun sayı / həll litrinin sayı = 1,2 mol CaCl2 / 2.905 L = 0.413080895
Nəticələrinizi qeyd edin. Nəticəni iki və ya üç vergüllə və ya müəlliminizin tələbi ilə yuvarlaqlaşdırmağı unutmayın. Nəticələri qeyd edərkən "molar konsentrasiyanı" "M" kimi qısaldın və sonra həll olunan maddənin kimyəvi simvolu.
- Misal üçün: 0.413 M CaCl2
Metod 4-dən 4: Əlavə Təcrübə
5.2 g NaCl 800 ml suda həll edildikdə məhlulun molar konsentrasiyasını hesablayın. Problemin verdiyi dəyərləri müəyyənləşdirin: kütlə qramda və həcm mililitrdə.
- Kütlə = 5.2 g NaCl
- Həcmi = 800 ml su
Na elementinin kub atomunu və Cl atom kubunu əlavə edərək NaCl-in kütlə molekulunu tapın.
- Kütlə atomu Na = 22,99 q
- Kütlə atomu Cl = 35.45 g
- Kütlə molekulları NaCl = 22.99 + 35.45 = 58.44 g
Solüsyonun kütləsini molar dönüşüm əmsalı ilə vurun. Bu nümunədə NaCl-in molekulyar kütləsi 58.44 q, çevrilmə əmsalı “1 mol / 58.44 g” dir.
- NaCl mol sayı = 5.2 g NaCl * (1 mol / 58.44 g) = 0.8898 mol = 0.09 mol
800 ml suyu 1000-ə bölün, suyun həcmini litrlə əldə edəcəksiniz.
- 800 ml-i 1 L / 1000 ml dönüşüm faktoru ilə mililitrdən litrə qədər də çoxaltmaq olar.
- Çarpma müddətini yuxarıdakı kimi qısaltmaq üçün onluq nöqtəni 3 rəqəmi sola qaytarmaq olar.
- Həcmi = 800 ml * (1 L / 1000 ml) = 800 ml / 1000 ml = 0.8 L
Solute mollarının sayını, litr həcmindəki həll həcminə bölün. Molyar konsentrasiyanı hesablamaq üçün 0,09 mol həll olunan maddəni (bu halda NaCl) litrə nisbətində həll etmək lazımdır.
- Molyar konsentrasiyası = həll olunan molun sayı / litr həll sayı = 0.09 mol / 0.8 L = 0.1125 mol / L
Son nəticəni qeyd edin. Nəticəni vergüldən sonra iki və ya üç ədədə yuvarlaqlaşdırın və "molar konsentrasiyası" nı "M" ilə həll olunan kimyəvi simvolu ilə qısaldın.
- Nəticə: 0.11 M NaCl