Müəllif:
Judy Howell
Yaradılış Tarixi:
2 İyul 2021
YeniləMə Tarixi:
21 İyun 2024

MəZmun
- Addımlamaq
- 2-nin 1-ci hissəsi: Atom nömrəsini tapmaq
- 2-nin 2-ci hissəsi: əlaqəli məlumat tapmaq
- Göstərişlər
Bir elementin atom sayı, bu elementin tək bir atomunun nüvəsindəki proton sayıdır. Bir elementin və ya izotopun atom sayı dəyişmir, buna görə atom nömrəsini bir elementin və ya izotopun neytron sayı kimi digər xüsusiyyətlərini hesablamaq üçün istifadə edə bilərsiniz.
Addımlamaq
2-nin 1-ci hissəsi: Atom nömrəsini tapmaq
 Dövri cədvəlin surətini tapın. Əlinizdə yoxdursa, birini tapa bilərsiniz. Hər bir elementin fərqli bir atom nömrəsi var, buna görə sürətli və asan metodlar mövcud deyil. Ya dövri cədvəlin surətini tapmalı, ya da birini yadda saxlamalısan.
Dövri cədvəlin surətini tapın. Əlinizdə yoxdursa, birini tapa bilərsiniz. Hər bir elementin fərqli bir atom nömrəsi var, buna görə sürətli və asan metodlar mövcud deyil. Ya dövri cədvəlin surətini tapmalı, ya da birini yadda saxlamalısan. - Əksər kimya dərsliklərinin üz qabığında dövri cədvəl var.
 Təhsil aldığınız elementi tapın. Əksər dövri cədvəllər müxtəlif elementlərin tam adlarını və kimyəvi simvollarını (civə üçün Hg kimi) ehtiva edir. Elementi tapmaqda çətinlik çəkirsinizsə, elementin adını və ardından "kimyəvi simvolu" onlayn axtarın.
Təhsil aldığınız elementi tapın. Əksər dövri cədvəllər müxtəlif elementlərin tam adlarını və kimyəvi simvollarını (civə üçün Hg kimi) ehtiva edir. Elementi tapmaqda çətinlik çəkirsinizsə, elementin adını və ardından "kimyəvi simvolu" onlayn axtarın.  Atom nömrəsini tapın. Atom nömrəsi ümumiyyətlə elementi ehtiva edən qutunun yuxarı sol və ya sağ küncündədir, ancaq qutunun başqa bir yerində də yerləşə bilər. Atom nömrəsi həmişə bir tamdır.
Atom nömrəsini tapın. Atom nömrəsi ümumiyyətlə elementi ehtiva edən qutunun yuxarı sol və ya sağ küncündədir, ancaq qutunun başqa bir yerində də yerləşə bilər. Atom nömrəsi həmişə bir tamdır. - Onluq rəqəmdirsə, ehtimal ki, atom kütləsinə baxırsınız.
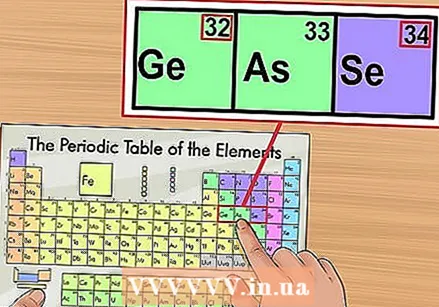 Qonşu elementlərə qarşı yoxlayın. Dövri cədvəl atom nömrəsi ilə sıralanır. Elementinizin atom nömrəsi "33" dirsə, soldakı element "32", sağdakı element isə "34" olmalıdır. Bu sifariş düzgündürsə, mütləq atom nömrəsini tapmısınız.
Qonşu elementlərə qarşı yoxlayın. Dövri cədvəl atom nömrəsi ilə sıralanır. Elementinizin atom nömrəsi "33" dirsə, soldakı element "32", sağdakı element isə "34" olmalıdır. Bu sifariş düzgündürsə, mütləq atom nömrəsini tapmısınız. - 56 (barium) və 88 (radium) elementlərindən sonra boş yer ola bilər. Əslində bir yer yoxdur; orada olan atom nömrələri olan elementlər sistemin qalan hissəsinin altındakı iki sətirdədir. Bu qədər ayrılmalarının yeganə səbəbi dövri cədvəlin daha az genişlənməsidir.
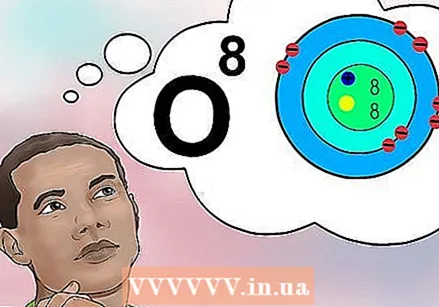 Atom nömrəsinin nə olduğunu anlayın. Bir elementin atom nömrəsi üçün sadə bir tərif var: bu elementin bir atomundakı proton sayı. Bu bir elementin əsas tərifidir. Protonların sayı, atomun neçə elektrona sahib olacağını təyin edən nüvənin ümumi elektrik yükünü təyin edir. Elektronlar, demək olar ki, bütün kimyəvi reaksiyalardan məsul olduqları üçün, atom sayı dolayı yolla bir elementin bütün fiziki və kimyəvi xüsusiyyətlərini təyin edir.
Atom nömrəsinin nə olduğunu anlayın. Bir elementin atom nömrəsi üçün sadə bir tərif var: bu elementin bir atomundakı proton sayı. Bu bir elementin əsas tərifidir. Protonların sayı, atomun neçə elektrona sahib olacağını təyin edən nüvənin ümumi elektrik yükünü təyin edir. Elektronlar, demək olar ki, bütün kimyəvi reaksiyalardan məsul olduqları üçün, atom sayı dolayı yolla bir elementin bütün fiziki və kimyəvi xüsusiyyətlərini təyin edir. - Başqa cür desək, səkkiz protonu olan hər atom bir oksigen atomudur. İki oksigen atomu fərqli sayda neytrona və ya biri iondursa fərqli sayda elektrona sahib ola bilər, lakin hər ikisi daima səkkiz protona sahib olacaqdır.
2-nin 2-ci hissəsi: əlaqəli məlumat tapmaq
 Atom ağırlığını tapmaq. Atom çəkisi adətən periyodik cədvəldə sözügedən elementin adı ilə yazılır və ümumiyyətlə iki və ya üç onluq yerə doğru hesablanır. Bu, təbiətdə tapmaq ehtimalı ilə uyğunlaşdırılan elementin bir atom orta kütləsidir. Bu rəqəm "atom kütlə vahidləri" ndədir (AMU (ingiliscə "atom kütlə vahidi" ndən)).
Atom ağırlığını tapmaq. Atom çəkisi adətən periyodik cədvəldə sözügedən elementin adı ilə yazılır və ümumiyyətlə iki və ya üç onluq yerə doğru hesablanır. Bu, təbiətdə tapmaq ehtimalı ilə uyğunlaşdırılan elementin bir atom orta kütləsidir. Bu rəqəm "atom kütlə vahidləri" ndədir (AMU (ingiliscə "atom kütlə vahidi" ndən)). - Bəzi elm adamları "atom çəkisi" əvəzinə "nisbi atom kütləsi" ifadəsini istifadə edirlər.
 Atom kütləsini anlayın. Atom kütləsi atom ağırlığına çox bənzər bir anlayışdır. Yeganə fərq, test nümunəsinin ortalaması əvəzinə müəyyən bir atomdan bəhs etməyinizdir. Bir qram dəmir kütlələri bir-birindən azca fərqlənən bir çox atom ehtiva edir, buna görə ortalamanı tapmaq üçün "nisbi ağırlıq" axtarırsınız. Yalnız bir xüsusi dəmir atomu ilə maraqlanırsınızsa, ortalama ilə maraqlanmırsınız - yalnız bu spesifik atomun dəqiq kütləsi sizi maraqlandırır.
Atom kütləsini anlayın. Atom kütləsi atom ağırlığına çox bənzər bir anlayışdır. Yeganə fərq, test nümunəsinin ortalaması əvəzinə müəyyən bir atomdan bəhs etməyinizdir. Bir qram dəmir kütlələri bir-birindən azca fərqlənən bir çox atom ehtiva edir, buna görə ortalamanı tapmaq üçün "nisbi ağırlıq" axtarırsınız. Yalnız bir xüsusi dəmir atomu ilə maraqlanırsınızsa, ortalama ilə maraqlanmırsınız - yalnız bu spesifik atomun dəqiq kütləsi sizi maraqlandırır. - Praktikada, atom kütləsi ümumiyyətlə yalnız bir atomu maraqlandıran kimya problemləri üçün verilir. Bu konsepsiyanı anlayın ki, atom ağırlığından fərqləndiyinə təəccüblənməyin.
 Kütlə nömrəsinə qədər dəyirmi. Kütlə sayı, bir elementin bir atomundakı protonların və neytronların ümumi sayını təşkil edir. Bu rəqəmi asanlıqla tapa bilərsiniz: yalnız dövri cədvəldə verilmiş atom çəkisini götürün və tam ədədi yuvarlaqlaşdırın.
Kütlə nömrəsinə qədər dəyirmi. Kütlə sayı, bir elementin bir atomundakı protonların və neytronların ümumi sayını təşkil edir. Bu rəqəmi asanlıqla tapa bilərsiniz: yalnız dövri cədvəldə verilmiş atom çəkisini götürün və tam ədədi yuvarlaqlaşdırın. - Neytronlar və protonlar həm 1 AMU, həm də elektronlar 0 AMU-ya yaxın olduğundan işləyir. Onluq ədədi əldə etmək üçün atomik çəki üçün dəqiq ölçmələrdən istifadə olunur, ancaq bizə yalnız proton və neytron sayını izah edən tam ədədlər maraqlıdır.
- Unutmayın ki, atom çəkisindən istifadə etmək sizə tipik bir nümunə üçün orta qiymət verəcəkdir. Brom nümunəsinin kütlə sayı 80-ə bərabərdir, ancaq göründüyü kimi, tək bir brom atomunun demək olar ki, həmişə 79 və ya 81 kütlə sayı var.
 Neytronların sayını hesablayın. Artıq atom sayının = proton sayının və kütlə sayının = proton sayı + neytron sayının olduğunu bilirsiniz. Bir elementdə neçə neytron olduğunu tapmaq üçün kütlə sayından atom nömrəsini çıxarmalısınız. Budur bir neçə nümunə:
Neytronların sayını hesablayın. Artıq atom sayının = proton sayının və kütlə sayının = proton sayı + neytron sayının olduğunu bilirsiniz. Bir elementdə neçə neytron olduğunu tapmaq üçün kütlə sayından atom nömrəsini çıxarmalısınız. Budur bir neçə nümunə: - Tək bir helium atomunun (He) kütlə sayı 4 və atom sayı 2-dir. Buna görə 4 - 2 = olmalıdır 2 neytron varı olmaq, Malik olmaq.
- Gümüş nümunəsinin (Ag) kütlə sayı 108-ə (dövri cədvələ görə) və atom nömrəsi 47-ə bərabərdir. Nümunədəki hər bir gümüş atomunun orta hesabla 108 - 47 = 61 neytronlar.
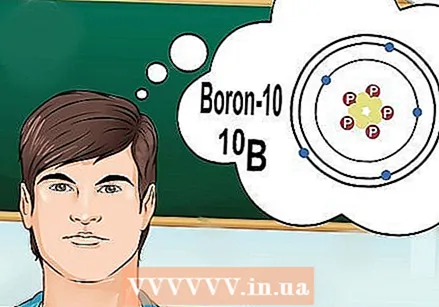 İzotopların nə olduğunu anlayın. İzotop, müəyyən sayda neytron olan bir elementin spesifik bir formasıdır. Kimya sualı "bor-10" və ya "B" -dən bəhs edildikdə, kütlə sayı 10 olan bor elementini nəzərdə tuturlar. "Tipik" bor dəyəri əvəzinə bu kütlə nömrəsini istifadə edin.
İzotopların nə olduğunu anlayın. İzotop, müəyyən sayda neytron olan bir elementin spesifik bir formasıdır. Kimya sualı "bor-10" və ya "B" -dən bəhs edildikdə, kütlə sayı 10 olan bor elementini nəzərdə tuturlar. "Tipik" bor dəyəri əvəzinə bu kütlə nömrəsini istifadə edin. - İzotopların fərqli bir atom nömrəsi yoxdur. Bir elementin hər bir izotopu eyni sayda protona malikdir.
Göstərişlər
- Bəzi ağır elementlər mötərizəyə və ya mötərizəyə daxil edilmiş atom ağırlığına malikdir. Bu o deməkdir ki, atom ağırlığı çoxlu izotopların ortalamasından çox, ən sabit izotopun dəqiq kütləsidir. (Bunun elementin atom nömrəsinə heç bir təsiri yoxdur.)