Müəllif:
Bobbie Johnson
Yaradılış Tarixi:
10 Aprel 2021
YeniləMə Tarixi:
1 İyul 2024

MəZmun
- Addımlar
- 2 -dən 1 -ci hissə: Avadanlıq hazırlayın
- 2 -ci hissə 2: Təcrübə aparın
- İpuçları
- Xəbərdarlıqlar
- Sənə nə lazımdır
Suyun parçalanması prosesi (H.2O) elektrik enerjisindən istifadə edərək (hidrogen və oksigen) tərkibinə elektroliz deyilir. Elektroliz nəticəsində əldə edilən qazlar tək başına istifadə edilə bilər - məsələn, hidrogen ən təmiz enerji mənbələrindən biri kimi xidmət edir. Bu prosesin adı bir qədər ağıllı görünsə də, doğru avadanlıqlara, biliklərə və bir az təcrübəyə sahib olsanız görünə biləcəyindən daha asandır.
Addımlar
2 -dən 1 -ci hissə: Avadanlıq hazırlayın
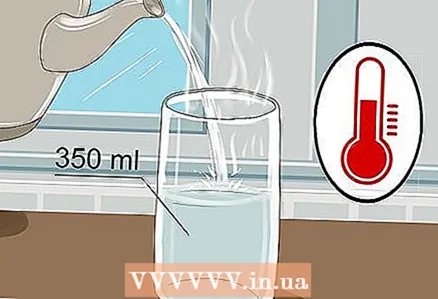 1 350 ml şüşə götürün və içinə isti su tökün. Şüşəni ağzına qədər doldurmağa ehtiyac yoxdur, bir az su kifayətdir. İsti su elektrik enerjisini daha yaxşı keçirsə də soyuq su edəcək.
1 350 ml şüşə götürün və içinə isti su tökün. Şüşəni ağzına qədər doldurmağa ehtiyac yoxdur, bir az su kifayətdir. İsti su elektrik enerjisini daha yaxşı keçirsə də soyuq su edəcək. - Həm musluk suyu, həm də şüşə suyu edəcək.
- İsti suyun daha aşağı viskoziteye malik olması ionların hərəkət etməsini asanlaşdırır.
 2 1 xörək qaşığı (20 qram) süfrə duzunu suda həll edin. Bir stəkana duz tökün və suyu həll etmək üçün qarışdırın. Bu, duzlu bir həll yaradacaq.
2 1 xörək qaşığı (20 qram) süfrə duzunu suda həll edin. Bir stəkana duz tökün və suyu həll etmək üçün qarışdırın. Bu, duzlu bir həll yaradacaq. - Sodyum xlorid (yəni masa duzu) suyun elektrik keçiriciliyini artıran bir elektrolitdir. Öz -özünə su elektrik enerjisini yaxşı keçirmir.
- Suyun elektrik keçiriciliyini artırdıqdan sonra, batareyanın yaratdığı cərəyan məhluldan daha asan keçəcək və molekulları hidrogen və oksigenə daha təsirli şəkildə parçalayacaq.
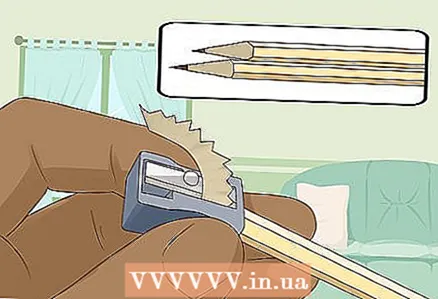 3 Qurğunu açmaq üçün hər iki ucunda iki yumşaq qələmi itiləyin. Qələmlərinizdən silgi çıxarmağı unutmayın. Bir qrafit çubuğu hər iki tərəfdən çıxmalıdır.
3 Qurğunu açmaq üçün hər iki ucunda iki yumşaq qələmi itiləyin. Qələmlərinizdən silgi çıxarmağı unutmayın. Bir qrafit çubuğu hər iki tərəfdən çıxmalıdır. - Qrafit çubuqlar, batareyanı bağladığınız izolyasiya edilmiş elektrodlar kimi xidmət edəcək.
- Qrafit bu təcrübə üçün çox uyğundur, çünki suda həll olunmur və korroziyaya uğramır.
 4 Şüşənin üstünə qoyulacaq qədər böyük bir karton vərəqi kəsin. İçərisində iki deşik açdıqdan sonra əyilməyən kifayət qədər qalın bir karton parçası istifadə edin. Ayaqqabı qutusundan və ya bənzərindən bir kvadrat parçanı kəsin.
4 Şüşənin üstünə qoyulacaq qədər böyük bir karton vərəqi kəsin. İçərisində iki deşik açdıqdan sonra əyilməyən kifayət qədər qalın bir karton parçası istifadə edin. Ayaqqabı qutusundan və ya bənzərindən bir kvadrat parçanı kəsin. - Karton, qələmləri şüşənin yanlarına və altına toxunmaması üçün suda saxlamaq üçün istifadə olunur.
- Karton keçiricidir, buna görə təhlükəsiz şəkildə bir şüşəyə qoya bilərsiniz.
 5 Kartonda iki deşik açmaq üçün qələmlərdən istifadə edin. Kartonu qələmlə deşin - bu vəziyyətdə sıx bağlanacaq və sürüşməyəcək. Qrafitin şüşənin yanlarına və ya altına toxunmadığından əmin olun, əks halda bu sınağa müdaxilə edəcək.
5 Kartonda iki deşik açmaq üçün qələmlərdən istifadə edin. Kartonu qələmlə deşin - bu vəziyyətdə sıx bağlanacaq və sürüşməyəcək. Qrafitin şüşənin yanlarına və ya altına toxunmadığından əmin olun, əks halda bu sınağa müdaxilə edəcək.
2 -ci hissə 2: Təcrübə aparın
 1 Timsah klipləri olan bir teli hər bir batareya terminalına bağlayın. Batareya elektrik cərəyanı mənbəyi kimi xidmət edəcək və sıxacları və qrafit çubuqları olan tellər vasitəsilə cərəyan suya çatacaq.Bir teli bir qısqacla pozitivə, digərini batareyanın mənfi terminalına bağlayın.
1 Timsah klipləri olan bir teli hər bir batareya terminalına bağlayın. Batareya elektrik cərəyanı mənbəyi kimi xidmət edəcək və sıxacları və qrafit çubuqları olan tellər vasitəsilə cərəyan suya çatacaq.Bir teli bir qısqacla pozitivə, digərini batareyanın mənfi terminalına bağlayın. - 6 voltluq bir batareya istifadə edin. Əgər yoxdursa, bunun əvəzinə 9 voltluq batareyadan istifadə edə bilərsiniz.
- Uyğun bir batareya bir elektrik təchizatı mağazasından və ya supermarketdən əldə edilə bilər.
 2 Tellərin digər uclarını qələmlərə bağlayın. Metal tel sıxaclarını qrafit çubuqlarına möhkəm bağlayın. Kliplərin qrafit çubuqlarından sürüşməməsi üçün qələmlərdən bir az daha ağac soymaq lazım ola bilər.
2 Tellərin digər uclarını qələmlərə bağlayın. Metal tel sıxaclarını qrafit çubuqlarına möhkəm bağlayın. Kliplərin qrafit çubuqlarından sürüşməməsi üçün qələmlərdən bir az daha ağac soymaq lazım ola bilər. - Beləliklə, dövrəni bağlayacaqsınız və batareyadan cərəyan sudan axacaq.
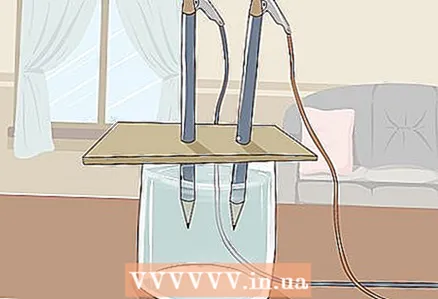 3 Kartonu şüşənin üzərinə qoyun ki, qələmlərin sərbəst ucları suya batsın. Karton vərəq şüşəyə söykənəcək qədər böyük olmalıdır. Qələmlərin düzgün yerləşdirilməsini pozmamaq üçün diqqətli olun.
3 Kartonu şüşənin üzərinə qoyun ki, qələmlərin sərbəst ucları suya batsın. Karton vərəq şüşəyə söykənəcək qədər böyük olmalıdır. Qələmlərin düzgün yerləşdirilməsini pozmamaq üçün diqqətli olun. - Təcrübənin uğurlu olması üçün qrafit şüşənin divarlarına və dibinə toxunmamalıdır. Bunu yenidən yoxlayın və lazım olduqda qələmləri düzəldin.
 4 Suyun hidrogen və oksigenə bölünməsinə baxın. Suya batırılmış qrafit çubuqlarından qaz baloncukları qalxmağa başlayacaq. Bunlar hidrogen və oksigendir. Hidrogen mənfi qütbdə, oksigen isə müsbət qütbdə ayrılacaq.
4 Suyun hidrogen və oksigenə bölünməsinə baxın. Suya batırılmış qrafit çubuqlarından qaz baloncukları qalxmağa başlayacaq. Bunlar hidrogen və oksigendir. Hidrogen mənfi qütbdə, oksigen isə müsbət qütbdə ayrılacaq. - Telləri batareyaya və qrafit çubuqlarına bağladığınız anda sudan elektrik cərəyanı axacaq.
- Mənfi qütbə bağlı olan qələm üzərində daha çox qaz baloncuğu əmələ gələcək, çünki hər bir su molekulu iki hidrogen atomu və bir oksigen atomundan ibarətdir.
İpuçları
- Qrafit şaftlı qələmləriniz yoxdursa, bunun yerinə iki kiçik teldən istifadə edə bilərsiniz. Hər telin bir ucunu müvafiq batareya dirəyinə sarın və digərini suya batırın. Nəticə qələmlə eyni olacaq.
- Fərqli bir batareya istifadə etməyə çalışın. Akan cərəyanın miqdarı batareyanın gərginliyindən asılıdır və bu da su molekullarının parçalanma sürətinə təsir göstərir.
Xəbərdarlıqlar
- Suya duz kimi bir elektrolit əlavə etsəniz, təcrübənin xlor kimi az miqdarda yan məhsul istehsal edəcəyini unutmayın. Bu qədər az miqdarda təhlükəsizdir, ancaq yüngül bir xlor qoxusu hiss edə bilərsiniz.
- Yetkinlərin nəzarəti altında bu təcrübəni həyata keçirin. Elektrik və qazlarla əlaqədardır və buna görə də təhlükəli ola bilər, baxmayaraq ki, mümkün deyil.
Sənə nə lazımdır
- İki sərt yumşaq qələm
- 6 və ya 9 voltluq bir batareya
- 350 mililitr həcmli şüşə
- Timsah klipləri olan 2 tel
- Qələm üçün itiləyici
- Duz