Müəllif:
Helen Garcia
Yaradılış Tarixi:
17 Aprel 2021
YeniləMə Tarixi:
1 İyul 2024
MəZmun
- Addımlar
- Metod 1 /2: Molarite vasitəsilə Normallığın Hesablanması
- Metod 2 /2: Ekvivalent Kütlədə Normallığın Hesablanması
- İpuçları
- Sənə nə lazımdır
Normallıq, məhlulda turşu və ya qələvinin konsentrasiyasını göstərir. Bir məhlulun normallığını öyrənmək üçün hesablamalarda həm molyarlıqdan, həm də molekulun ekvivalent kütləsindən istifadə etmək olar. Əgər molyarlıqdan istifadə etməyi seçsəniz, M = mo (mo) və n - hidrogen və ya hidroksid molekullarının sayı olan N = M (n) düsturundan istifadə edin. Ekvivalent kütləni istifadə etmək qərarına gəlsəniz, N = eq ÷ V düsturundan istifadə edin, burada eq ekvivalentlərin sayıdır və V məhlulun həcmidir.
Addımlar
Metod 1 /2: Molarite vasitəsilə Normallığın Hesablanması
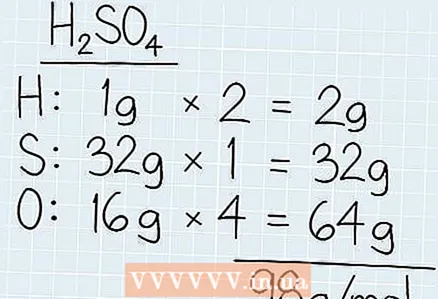 1 Solüsyonun bütün komponentlərinin molar kütləsini əlavə edin. Dövri cədvəldə kimyəvi formulun elementlərini taparaq onların molar kütləsinə uyğun olan atom kütləsini tapın. Hər bir elementin molar kütləsini yazın və bu elementlərin sayına vurun. Ümumi molar kütləsini tapmaq üçün bütün komponentlərin molar kütləsini əlavə edin.
1 Solüsyonun bütün komponentlərinin molar kütləsini əlavə edin. Dövri cədvəldə kimyəvi formulun elementlərini taparaq onların molar kütləsinə uyğun olan atom kütləsini tapın. Hər bir elementin molar kütləsini yazın və bu elementlərin sayına vurun. Ümumi molar kütləsini tapmaq üçün bütün komponentlərin molar kütləsini əlavə edin. - Məsələn, kükürd turşusunun molar kütləsini bilmək istəyirsinizsə (H2BELƏ Kİ4), hidrogen (1 g), kükürd (3 g) və oksigenin (16 q) molar kütləsini tapın.
- Kütləni kompozisiyadakı komponentlərin sayına vurun. Misalımızda 2 hidrogen atomu və 4 oksigen atomu var. Hidrogenin ümumi molar kütləsi 2 x 1 g = 2 q -dır.Bu məhlulda oksigenin molar kütləsi 4 x 16 g = 64 q olacaq.
- Bütün molar kütlələri birlikdə əlavə edin. 2 g + 32 g + 64 g = 98 g / mol alırsınız.
- Axtardığınız həllin molaritesini artıq bilirsinizsə, birbaşa 4 -cü addıma keçin.
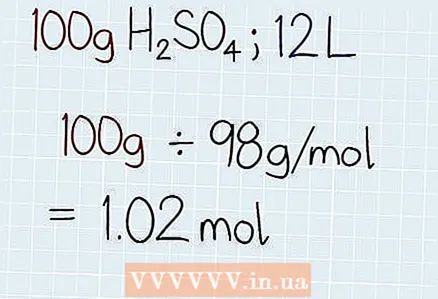 2 Solüsyonun həqiqi kütləsini molar kütləsinə bölün. Çözümün həqiqi çəkisini öyrənin. Ya həll olan qabda, ya da vəzifənin özündə göstəriləcək.Sonra həll kütləsini əvvəllər tapılan ümumi molar kütləyə bölün. Nəticədə məhluldakı molların sayı olacaq, bundan sonra "mol" yazılmalıdır.
2 Solüsyonun həqiqi kütləsini molar kütləsinə bölün. Çözümün həqiqi çəkisini öyrənin. Ya həll olan qabda, ya da vəzifənin özündə göstəriləcək.Sonra həll kütləsini əvvəllər tapılan ümumi molar kütləyə bölün. Nəticədə məhluldakı molların sayı olacaq, bundan sonra "mol" yazılmalıdır. - Məsələn, 100 g H normasını öyrənməyə çalışırsınızsa2BELƏ Kİ412 litr maye içərisində həll olunaraq həqiqi kütləni istifadə edin və molar ilə bölün. Nəticədə əldə edəcəksiniz: 100 g ÷ 98 g / mol = 1.02 mol.
- 1 mol 6.02 x 10 atom və ya bir həll molekuluna bərabərdir.
 3 Molariteyi öyrənmək üçün nəticəni məhlulun həcminə bölün. Yeni hesablanmış məhluldakı molların sayını götürün və ölçülməli olan məhlulun ümumi həcminə bölün. Nəticədə, məhlulun konsentrasiyasını öyrənə biləcəyiniz molyarlığı (M) biləcəksiniz.
3 Molariteyi öyrənmək üçün nəticəni məhlulun həcminə bölün. Yeni hesablanmış məhluldakı molların sayını götürün və ölçülməli olan məhlulun ümumi həcminə bölün. Nəticədə, məhlulun konsentrasiyasını öyrənə biləcəyiniz molyarlığı (M) biləcəksiniz. - Nümunəmizə əsaslanaraq aşağıdakı düsturu əldə edirik: 1.02 mol ÷ 12 L = 0.085 M.
Məsləhət: həll etməmişsinizsə, həll həcmini litrə çevirməyinizə əmin olun. Əks təqdirdə səhv cavab alacaqsınız.
 4 Molariteyi hidrogen və ya hidroksid molekullarının sayına vurun. Bir turşudakı hidrogen atomlarının (H) və ya bazdakı (OH) hidroksid molekullarının sayını öyrənmək üçün kimyəvi formula baxın. Daha sonra normal konsentrasiyanı və ya normallığı tapmaq üçün məhlulun molyarlığını həmin məhluldakı hidrogen və ya hidroksid molekullarının sayına vurun. Cavabınızın sonunda "N" qısaltmasını yazın.
4 Molariteyi hidrogen və ya hidroksid molekullarının sayına vurun. Bir turşudakı hidrogen atomlarının (H) və ya bazdakı (OH) hidroksid molekullarının sayını öyrənmək üçün kimyəvi formula baxın. Daha sonra normal konsentrasiyanı və ya normallığı tapmaq üçün məhlulun molyarlığını həmin məhluldakı hidrogen və ya hidroksid molekullarının sayına vurun. Cavabınızın sonunda "N" qısaltmasını yazın. - Misalımızda kükürd turşusu (H2BELƏ Kİ4) 2 hidrogen atomu. Düstur belə olacaq: 0.085 M x 2 = 0.17 N.
- Başqa bir nümunədə, 2 M molyarlığı olan natrium hidroksid (NaOH) yalnız 1 hidroksid molekuluna malikdir. Buna görə düstur aşağıdakı kimi olacaq: 2 M x 1 = 2 N.
Metod 2 /2: Ekvivalent Kütlədə Normallığın Hesablanması
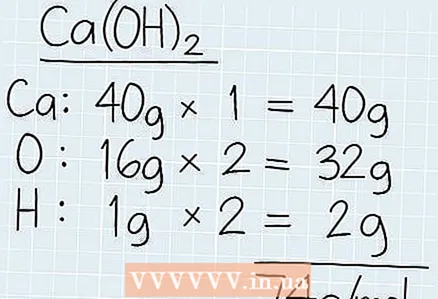 1 Solüsyonun ümumi molar kütləsini tapın. Çözümün kimyəvi formuluna nəzər salın və dövri cədvəldə hər bir elementi tapın. Hər bir elementin molar kütləsini yazın və düsturdakı elementlərin sayına vurun. Qütbdəki molar kütləni tapmaq üçün bütün molar kütlələri əlavə edin.
1 Solüsyonun ümumi molar kütləsini tapın. Çözümün kimyəvi formuluna nəzər salın və dövri cədvəldə hər bir elementi tapın. Hər bir elementin molar kütləsini yazın və düsturdakı elementlərin sayına vurun. Qütbdəki molar kütləni tapmaq üçün bütün molar kütlələri əlavə edin. - Məsələn, Ca (OH) molar kütləsini bilmək istəyirsinizsə.2, sonra kalsium (40 q), oksigen (16 q) və hidrogenin (1 q) molar kütləsini tapın.
- Formulda 2 oksigen və hidrogen atomu var. Ümumi oksigen kütləsi: 2 x 16 g = 32 q, Hidrogenin molar kütləsi: 2 x 1 g = 2 q olacaq.
- 40 g + 32 g + 2 g = 74 g / mol almaq üçün bütün molar kütlələri əlavə edin.
 2 Molar kütləsini hidrogen və ya hidroksid molekullarının sayına bölün. Bazdakı bir turşu və ya hidroksid (OH) molekullarında hidrogen atomlarının (H) sayını öyrənin. Alınan ümumi molar kütləni 1 mol hidrogen və ya hidroksidin kütləsinə bərabər olacaq 1 ekvivalentin ağırlığını tapmaq üçün atom və ya molekul sayına bölün. Cavabın sonunda ekvivalent kütləsi mənasını verən "G.-e." qısaltmasını yazın.
2 Molar kütləsini hidrogen və ya hidroksid molekullarının sayına bölün. Bazdakı bir turşu və ya hidroksid (OH) molekullarında hidrogen atomlarının (H) sayını öyrənin. Alınan ümumi molar kütləni 1 mol hidrogen və ya hidroksidin kütləsinə bərabər olacaq 1 ekvivalentin ağırlığını tapmaq üçün atom və ya molekul sayına bölün. Cavabın sonunda ekvivalent kütləsi mənasını verən "G.-e." qısaltmasını yazın. - Bizim nümunəmizdə Ca (OH)2 2 iki hidrogen molekulu, yəni ekvivalentinin kütləsi 74 q / mol-a bərabər olacaq ÷ 2 = 37 G.-e.
 3 Çözümün həqiqi ağırlığını ekvivalent çəkiyə bölün. Ekvivalentin kütləsini bildikdən sonra, həll olan konteynerdə və ya həll olunan problemdə göstərilən məhlulun kütləsinə bölün. Cavab həllində ekvivalentlərin sayı olacaq, beləliklə normallığı hesablaya bilərsiniz. Cavabın sonunda "e" qısaltmasını qoyun.
3 Çözümün həqiqi ağırlığını ekvivalent çəkiyə bölün. Ekvivalentin kütləsini bildikdən sonra, həll olan konteynerdə və ya həll olunan problemdə göstərilən məhlulun kütləsinə bölün. Cavab həllində ekvivalentlərin sayı olacaq, beləliklə normallığı hesablaya bilərsiniz. Cavabın sonunda "e" qısaltmasını qoyun. - Əgər nümunəmizdə 75 q Ca (OH)2, onda düstur aşağıdakı kimi olacaq: 75 g ÷ 37 G.-e = 2.027 Oe.
 4 Ekvivalentlərin sayını məhlulun litrlə bölün. Çözümün ümumi həcmini tapın və cavabı litrlərlə yazın. Yeni əldə edilən ekvivalentlərin sayını götürün və həllinin həcminə bölün, normallığı tapın. Cavabınızın sonunda "N" qısaltması qoyun.
4 Ekvivalentlərin sayını məhlulun litrlə bölün. Çözümün ümumi həcmini tapın və cavabı litrlərlə yazın. Yeni əldə edilən ekvivalentlərin sayını götürün və həllinin həcminə bölün, normallığı tapın. Cavabınızın sonunda "N" qısaltması qoyun. - 8 litr həcmli bir məhlulda 75 q Ca (OH) varsa2, sonra ekvivalentlərin sayını həcmə aşağıdakı şəkildə bölün: 2.027 Oe. ÷ 8 l = 0,253 N.
İpuçları
- Normal konsentrasiya və ya normallıq, turşuları və əsasları ölçmək üçün istifadə olunur. Başqa bir məhlulun konsentrasiyasını təyin etmək lazımdırsa, bu ümumiyyətlə molyarlığı ölçməklə aparılır.
Sənə nə lazımdır
- Dövri Cədvəl
- Kalkulyator