Müəllif:
Sara Rhodes
Yaradılış Tarixi:
12 Fevral 2021
YeniləMə Tarixi:
28 İyun 2024

MəZmun
- Addımlar
- 2 -ci hissə 1: Kimya qanunlarına görə oksidləşmə vəziyyətinin təyin edilməsi
- 2 -ci hissə 2: Kimya qanunlarından istifadə etmədən oksidləşmə vəziyyətinin təyin edilməsi
- İpuçları
- Sənə nə lazımdır
Kimyada "oksidləşmə" və "azalma" anlayışları, bir atomun və ya bir qrup atomun elektron itirdiyi və ya qazandığı reaksiyalar deməkdir. Oksidləşmə vəziyyəti, yenidən bölüşdürülmüş elektronların sayını xarakterizə edən və bu elektronların bir reaksiya zamanı atomlar arasında necə paylandığını göstərən bir və ya daha çox atomlara verilən ədədi dəyərdir. Bu dəyərin təyin edilməsi, atomlardan və onlardan ibarət olan molekullardan asılı olaraq həm sadə, həm də olduqca mürəkkəb bir prosedur ola bilər. Üstəlik, bəzi elementlərin atomları bir neçə oksidləşmə vəziyyətinə malik ola bilər. Xoşbəxtlikdən, oksidləşmə vəziyyətini təyin etmək üçün sadə birmənalı qaydalar var ki, onların inamlı istifadəsi üçün kimya və cəbrin əsaslarını bilmək kifayətdir.
Addımlar
2 -ci hissə 1: Kimya qanunlarına görə oksidləşmə vəziyyətinin təyin edilməsi
 1 Sözügedən maddənin elementar olub olmadığını müəyyənləşdirin. Kimyəvi birləşmənin xaricindəki atomların oksidləşmə vəziyyəti sıfırdır. Bu qayda həm ayrı sərbəst atomlardan əmələ gələn maddələr, həm də bir elementin iki və ya çox atomlu molekullarından ibarət olanlar üçün doğrudur.
1 Sözügedən maddənin elementar olub olmadığını müəyyənləşdirin. Kimyəvi birləşmənin xaricindəki atomların oksidləşmə vəziyyəti sıfırdır. Bu qayda həm ayrı sərbəst atomlardan əmələ gələn maddələr, həm də bir elementin iki və ya çox atomlu molekullarından ibarət olanlar üçün doğrudur. - Məsələn, Al(s) və Cl2 0 oksidləşmə vəziyyətinə malikdir, çünki hər ikisi kimyəvi cəhətdən bağlı olmayan bir elementar vəziyyətdədir.
- Qeyd edək ki, kükürdün allotropik forması S8və ya octacera, atipik quruluşuna baxmayaraq, sıfır oksidləşmə vəziyyəti ilə də xarakterizə olunur.
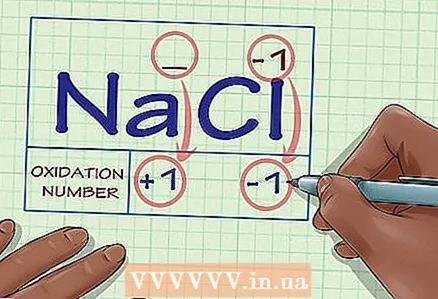 2 Söz mövzusu maddənin ionlardan ibarət olub olmadığını müəyyənləşdirin. İonların oksidləşmə vəziyyəti yüklərinə bərabərdir. Bu həm sərbəst ionlar, həm də kimyəvi birləşmələrin bir hissəsi olanlar üçün doğrudur.
2 Söz mövzusu maddənin ionlardan ibarət olub olmadığını müəyyənləşdirin. İonların oksidləşmə vəziyyəti yüklərinə bərabərdir. Bu həm sərbəst ionlar, həm də kimyəvi birləşmələrin bir hissəsi olanlar üçün doğrudur. - Məsələn, Cl ionunun oksidləşmə vəziyyəti -1 -dir.
- NaCl kimyəvi birləşməsindəki Cl ionunun oksidləşmə vəziyyəti də -1 -dir. Na ionunun tərifi ilə +1 yükü olduğu üçün Cl ionunun yükünün -1, beləliklə oksidləşmə vəziyyətinin -1 olduğu qənaətinə gəlirik.
 3 Unutmayın ki, metal ionları bir neçə oksidləşmə vəziyyətinə malik ola bilər. Bir çox metal elementin atomları fərqli miqdarda ionlaşa bilir. Məsələn, dəmir (Fe) kimi bir metalın ion yükü +2 və ya +3 təşkil edir. Metal ionlarının yükü (və oksidləşmə vəziyyəti) bu metalın kimyəvi birləşmənin bir hissəsi olduğu digər elementlərin ionlarının yükləri ilə müəyyən edilə bilər; mətndə bu yük Roma rəqəmləri ilə ifadə olunur: məsələn, dəmir (III) +3 oksidləşmə vəziyyətinə malikdir.
3 Unutmayın ki, metal ionları bir neçə oksidləşmə vəziyyətinə malik ola bilər. Bir çox metal elementin atomları fərqli miqdarda ionlaşa bilir. Məsələn, dəmir (Fe) kimi bir metalın ion yükü +2 və ya +3 təşkil edir. Metal ionlarının yükü (və oksidləşmə vəziyyəti) bu metalın kimyəvi birləşmənin bir hissəsi olduğu digər elementlərin ionlarının yükləri ilə müəyyən edilə bilər; mətndə bu yük Roma rəqəmləri ilə ifadə olunur: məsələn, dəmir (III) +3 oksidləşmə vəziyyətinə malikdir. - Nümunə olaraq alüminium ionu olan bir birləşməni nəzərdən keçirək. AlCl birləşməsinin ümumi yükü3 sıfırdır.Cl ionlarının yükünün -1 olduğunu və birləşmənin 3 belə iondan ibarət olduğunu bildiyimizdən, sözügedən maddənin ümumi neytrallığı üçün Al ionunun +3 yükü olmalıdır. Beləliklə, bu vəziyyətdə alüminiumun oksidləşmə vəziyyəti +3 -dir.
 4 Oksigenin oksidləşmə vəziyyəti -2 -dir (bəzi istisnalar istisna olmaqla). Demək olar ki, bütün hallarda oksigen atomları -2 oksidləşmə vəziyyətinə malikdir. Bu qaydanın bir neçə istisnası var:
4 Oksigenin oksidləşmə vəziyyəti -2 -dir (bəzi istisnalar istisna olmaqla). Demək olar ki, bütün hallarda oksigen atomları -2 oksidləşmə vəziyyətinə malikdir. Bu qaydanın bir neçə istisnası var: - Əgər oksigen elementar vəziyyətdədirsə (O2), digər elementar maddələrdə olduğu kimi oksidləşmə vəziyyəti də 0 -dır.
- Əgər oksigen bir hissəsidirsə peroksid, oksidləşmə vəziyyəti -1 -dir. Peroksidlər sadə oksigen-oksigen bağı (yəni peroksid anyonu O) olan bir qrup birləşmələrdir2). Məsələn, H2O2 (hidrogen peroksid) oksigenin yükü və oksidləşmə vəziyyəti -1 -dir.
- Flüor ilə birləşdirildikdə oksigen +2 oksidləşmə vəziyyətinə malikdir, aşağıdakı flor qaydasını oxuyun.
 5 Hidrogen bir az istisna olmaqla +1 oksidləşmə vəziyyətinə malikdir. Oksigen kimi, istisnalar da var. Bir qayda olaraq, hidrogenin oksidləşmə vəziyyəti +1 -dir (elementar vəziyyətdə deyilsə H2). Lakin hidrid adlanan birləşmələrdə hidrogenin oksidləşmə vəziyyəti -1 -dir.
5 Hidrogen bir az istisna olmaqla +1 oksidləşmə vəziyyətinə malikdir. Oksigen kimi, istisnalar da var. Bir qayda olaraq, hidrogenin oksidləşmə vəziyyəti +1 -dir (elementar vəziyyətdə deyilsə H2). Lakin hidrid adlanan birləşmələrdə hidrogenin oksidləşmə vəziyyəti -1 -dir. - Məsələn, H.2O Hidrogen oksidləşmə vəziyyəti +1 -dir, çünki oksigen atomu -2 yükə malikdir və ümumi neytrallıq üçün iki +1 yük tələb olunur. Buna baxmayaraq, sodyum hidridin tərkibində hidrogen oksidləşmə vəziyyəti artıq -1 -dir, çünki Na ionu +1, ümumi elektron neytrallığı üçün isə hidrogen atomunun yükü (və beləliklə oksidləşmə vəziyyəti) olmalıdır. ol -1.
 6 Florin həmişə -1 oksidləşmə vəziyyətinə malikdir. Artıq qeyd edildiyi kimi, bəzi elementlərin (metal ionları, peroksidlərdəki oksigen atomları və s.) Oksidləşmə vəziyyəti bir çox amillərdən asılı olaraq dəyişə bilər. Flüorun oksidləşmə vəziyyəti dəyişməz olaraq -1 -dir. Bunun səbəbi, bu elementin ən böyük elektronegativliyə malik olmasıdır - başqa sözlə, flor atomları öz elektronları ilə ayrılmaq və xarici elektronları ən çox cəlb etmək istəmirlər. Beləliklə, onların ittihamı dəyişməz olaraq qalır.
6 Florin həmişə -1 oksidləşmə vəziyyətinə malikdir. Artıq qeyd edildiyi kimi, bəzi elementlərin (metal ionları, peroksidlərdəki oksigen atomları və s.) Oksidləşmə vəziyyəti bir çox amillərdən asılı olaraq dəyişə bilər. Flüorun oksidləşmə vəziyyəti dəyişməz olaraq -1 -dir. Bunun səbəbi, bu elementin ən böyük elektronegativliyə malik olmasıdır - başqa sözlə, flor atomları öz elektronları ilə ayrılmaq və xarici elektronları ən çox cəlb etmək istəmirlər. Beləliklə, onların ittihamı dəyişməz olaraq qalır.  7 Bir birləşmədə oksidləşmə vəziyyətlərinin cəmi onun yükünə bərabərdir. Kimyəvi bir birləşmə meydana gətirən bütün atomların oksidləşmə vəziyyətləri bu birləşmənin yükünü artırmalıdır. Məsələn, bir birləşmə neytral olarsa, onun bütün atomlarının oksidləşmə vəziyyətlərinin cəmi sıfır olmalıdır; birləşmə -1 yüklü çox atomlu bir iondursa, oksidləşmə vəziyyətlərinin cəmi -1 -dir və s.
7 Bir birləşmədə oksidləşmə vəziyyətlərinin cəmi onun yükünə bərabərdir. Kimyəvi bir birləşmə meydana gətirən bütün atomların oksidləşmə vəziyyətləri bu birləşmənin yükünü artırmalıdır. Məsələn, bir birləşmə neytral olarsa, onun bütün atomlarının oksidləşmə vəziyyətlərinin cəmi sıfır olmalıdır; birləşmə -1 yüklü çox atomlu bir iondursa, oksidləşmə vəziyyətlərinin cəmi -1 -dir və s. - Bu yaxşı bir test üsuludur - oksidləşmə vəziyyətlərinin cəmi birləşmənin ümumi yükünə bərabər deyilsə, deməli bir yerdə səhv edirsiniz.
2 -ci hissə 2: Kimya qanunlarından istifadə etmədən oksidləşmə vəziyyətinin təyin edilməsi
 1 Oksidləşmə vəziyyəti ilə bağlı ciddi qaydaları olmayan atomları tapın. Bəzi elementlər üçün oksidləşmə vəziyyətini tapmaq üçün qəti şəkildə qurulmuş qaydalar yoxdur. Bir atom yuxarıda sadalanan qaydalardan heç birinə uyğun gəlmirsə və onun yükünü bilmirsinizsə (məsələn, atom kompleksin bir hissəsidir və yükü göstərilməyib), belə bir atomun oksidləşmə vəziyyətini təyin edə bilərsiniz. istisna olmaqla. Əvvəlcə birləşmənin bütün digər atomlarının yükünü təyin edin və sonra birləşmənin məlum ümumi yükündən bu atomun oksidləşmə vəziyyətini hesablayın.
1 Oksidləşmə vəziyyəti ilə bağlı ciddi qaydaları olmayan atomları tapın. Bəzi elementlər üçün oksidləşmə vəziyyətini tapmaq üçün qəti şəkildə qurulmuş qaydalar yoxdur. Bir atom yuxarıda sadalanan qaydalardan heç birinə uyğun gəlmirsə və onun yükünü bilmirsinizsə (məsələn, atom kompleksin bir hissəsidir və yükü göstərilməyib), belə bir atomun oksidləşmə vəziyyətini təyin edə bilərsiniz. istisna olmaqla. Əvvəlcə birləşmənin bütün digər atomlarının yükünü təyin edin və sonra birləşmənin məlum ümumi yükündən bu atomun oksidləşmə vəziyyətini hesablayın. - Məsələn, Na tərkibində2BELƏ Kİ4 kükürd atomunun (S) yükü məlum deyil - yalnız bilirik ki, kükürd elementar vəziyyətdə deyil. Bu birləşmə oksidləşmə vəziyyətini təyin etmək üçün cəbr üsulunu göstərmək üçün yaxşı bir nümunə kimi xidmət edir.
 2 Kompozisiyada qalan elementlərin oksidləşmə dərəcələrini tapın. Yuxarıda təsvir olunan qaydalardan istifadə edərək, birləşmənin qalan atomlarının oksidləşmə dərəcələrini təyin edin. O, H və sair qaydaların istisnalarını unutma.
2 Kompozisiyada qalan elementlərin oksidləşmə dərəcələrini tapın. Yuxarıda təsvir olunan qaydalardan istifadə edərək, birləşmənin qalan atomlarının oksidləşmə dərəcələrini təyin edin. O, H və sair qaydaların istisnalarını unutma. - Na üçün2BELƏ Kİ4, qaydalarımızdan istifadə edərək, Na ionunun yükünün (və buna görə də oksidləşmə vəziyyətinin) +1 olduğunu və oksigen atomlarının hər biri üçün -2 olduğunu görürük.
 3 Atomların sayını oksidləşmə vəziyyətinə görə vurun. İndi bir atomdan başqa bütün atomların oksidləşmə vəziyyətlərini bildiyimiz üçün bəzi elementlərin bir neçə atomunun ola biləcəyini nəzərə almaq lazımdır. Hər bir elementin atomlarının sayını (birləşmənin kimyəvi formulunda elementin simvolunu izləyən bir alt simvol olaraq göstərilmişdir) oksidləşmə vəziyyətinə vurun.
3 Atomların sayını oksidləşmə vəziyyətinə görə vurun. İndi bir atomdan başqa bütün atomların oksidləşmə vəziyyətlərini bildiyimiz üçün bəzi elementlərin bir neçə atomunun ola biləcəyini nəzərə almaq lazımdır. Hər bir elementin atomlarının sayını (birləşmənin kimyəvi formulunda elementin simvolunu izləyən bir alt simvol olaraq göstərilmişdir) oksidləşmə vəziyyətinə vurun. - Na -da2BELƏ Kİ4 2 Na atomu və 4 O atomumuz var. Beləliklə, 2 × +1 vuraraq bütün Na atomlarının (2) oksidləşmə vəziyyətini və 4 × -2 -O (-8) atomlarının oksidləşmə vəziyyətini alırıq.
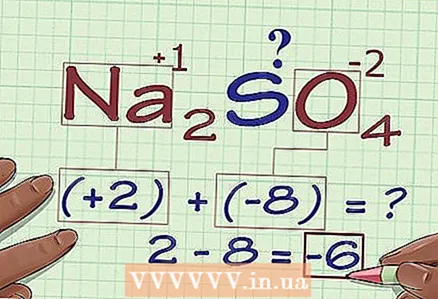 4 Əvvəlki nəticələri əlavə edin. Çarpmanın nəticələrini yekunlaşdıraraq, birləşmənin oksidləşmə vəziyyətini alırıq olmadan istədiyiniz atomun qatqısı nəzərə alınmaqla.
4 Əvvəlki nəticələri əlavə edin. Çarpmanın nəticələrini yekunlaşdıraraq, birləşmənin oksidləşmə vəziyyətini alırıq olmadan istədiyiniz atomun qatqısı nəzərə alınmaqla. - Nümunəmizdə Na üçün2BELƏ Kİ4 2 və -8 əlavə edirik və -6 alırıq.
 5 Bileşik yükündən bilinməyən oksidləşmə vəziyyətini tapın. İstədiyiniz oksidləşmə vəziyyətini asanlıqla hesablamaq üçün bütün məlumatlarınız var. Sol tərəfində əvvəlki hesablama addımında əldə edilən ədədin və bilinməyən oksidləşmə vəziyyətinin cəminin və birləşmənin ümumi yükünün sağ tərəfində olacaq bir tənlik yazın. Başqa sözlə, (Məlum oksidləşmə vəziyyətlərinin cəmi) + (arzu olunan oksidləşmə vəziyyəti) = (Bir maddənin yükü).
5 Bileşik yükündən bilinməyən oksidləşmə vəziyyətini tapın. İstədiyiniz oksidləşmə vəziyyətini asanlıqla hesablamaq üçün bütün məlumatlarınız var. Sol tərəfində əvvəlki hesablama addımında əldə edilən ədədin və bilinməyən oksidləşmə vəziyyətinin cəminin və birləşmənin ümumi yükünün sağ tərəfində olacaq bir tənlik yazın. Başqa sözlə, (Məlum oksidləşmə vəziyyətlərinin cəmi) + (arzu olunan oksidləşmə vəziyyəti) = (Bir maddənin yükü).- Bizim vəziyyətimizdə Na2BELƏ Kİ4 həll belə görünür:
- (Məlum oksidləşmə vəziyyətlərinin cəmi) + (arzu olunan oksidləşmə vəziyyəti) = (mürəkkəb yük)
- -6 + S = 0
- S = 0 + 6
- S = 6. V Na2BELƏ Kİ4 kükürd oksidləşmə vəziyyətinə malikdir 6.
- Bizim vəziyyətimizdə Na2BELƏ Kİ4 həll belə görünür:
İpuçları
- Birləşmələrdə bütün oksidləşmə vəziyyətlərinin cəmi yükə bərabər olmalıdır. Məsələn, birləşmə iki atomlu bir iondursa, atomların oksidləşmə vəziyyətlərinin cəmi ümumi ion yükünə bərabər olmalıdır.
- Dövri cədvəldən istifadə etmək və metal və qeyri-metal elementlərin harada yerləşdiyini bilmək çox faydalıdır.
- Elementar formada olan atomların oksidləşmə vəziyyəti həmişə sıfırdır. Tək bir ionun oksidləşmə vəziyyəti onun yükünə bərabərdir. Hidrogen, litium, natrium kimi dövri cədvəlin 1A qrupunun elementləri elementar formada +1 oksidləşmə vəziyyətinə malikdir; Maqnezium və kalsium kimi 2A qrupu metalların oksidləşmə vəziyyəti elementar formada +2 -dir. Kimyəvi bağ növündən asılı olaraq oksigen və hidrogen 2 fərqli oksidləşmə vəziyyətinə malik ola bilər.
Sənə nə lazımdır
- Elementlərin dövri cədvəli
- İnternetə daxil olmaq və ya kimya haqqında məlumat kitabları
- Bir kağız vərəqi, qələm və ya qələm
- Kalkulyator



